사업공고
home 알림마당 사업공고
- 글자크기
2020년도 국산의료기기 신제품 사용자(의료기관) 평가 지원사업 공고(~2020.1.31)
| 작성자 | 관리자 | ||
|---|---|---|---|
| 작성일 | 2019-12-23 | 조회수 | 10,190 |
| 첨부파일 | |||
국산의료기기 신제품 사용자(의료기관) 평가 지원사업 공고
2020년도『국산의료기기 신제품 사용자(의료기관) 평가 지원 사업』을 수행할 기관을 다음과 같이 공모하오니 관련 의료기관 및 기업체의 적극적인 참여를 바랍니다.
1. 사업 개요
□ 국산 신제품의 브랜드 인지도와 신뢰도 확보를 위해 혁신기술 등이 적용된 신제품 사용자(의료기관) 평가 지원
○ 수입 제품 사용 비중이 높은 국내 주요 의료기관을 통해 국산 유망 신제품의 평가 및 시장진입을 지원
- 의료기관 사용자(의료진)의 평가를 통한 국산 신제품의 우수성 검증 및 성능 개선
○ 브랜드 파워가 있는 의료기관의 신제품 평가 결과를 적극 홍보하여, 중소 의료기기기업 제품의 브랜드 인지도 강화, 대학병원 진출, 수출 확대를 통한 시장진출 지원
< 국산의료기기 신제품 사용자(의료기관) 평가 예시 > • 의료기관의 기존 사용제품과 신제품 간의 비교평가(결과는 국산 제품의 마케팅‧홍보 등에 활용) • 국산 신제품의 성능 검증 및 개선사항을 도출하기 위한 평가 • 보험등재 등 근거자료를 마련하기 위한 국산 신제품의 치료효과 등의 검증평가 |
< 국산의료기기 신제품 사용자(의료기관) 평가 지원 체계>
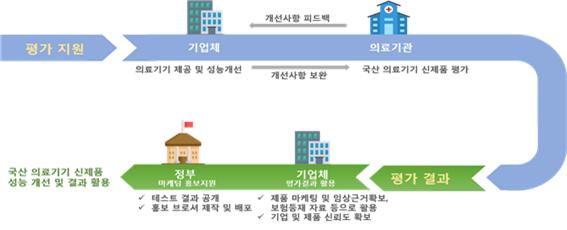
□ 지원기간 및 비용
○ 사업 기간 : 2020년 3월∼11월(9개월)
* 제품의 특성 및 제품 평가 방법에 따라 사업기간은 최대 2년까지 지원 가능(지원 과제의 30% 이내로 선정)
* 2차년도 지원은 ‘20년 말 연차평가를 통해 계속 지원여부를 결정
○ 지원 금액
- (단년) 최대 7,500만원/연 이내
- (다년) 최대 15,000만원/2년 이내
* 다년 사업의 경우, 1차년도 7,500만원/연 이내 지원으로 2차년 지원 금액은 1차년 지원금과 동일
2. 사업 내용
□ 지원 대상
○ (지원기관) 주관기관(의료기관)과 참여기업(제조기업)으로 구성된 컨소시엄
- 주관기관 : 상급종합병원(의료법 제3조의4), 종합병원(의료법 제3조의3), 전문병원(의료법 제3조5)
* 대학병원, 치과대학병원, 한의과대학병원 등 식품의약품안전처에서 지정한 임상시험실시기관을 포함
- 참여기업 : 평가 대상 제품을 제조한 국내 제조기업(중소기업 등)
○ (지원 제품) 식약처 의료기기 제조 허가·인증 및 신고 후 시장 진입을 준비 중이거나 판매 초기인 국산 신제품*
- 국내 종합병원 이상(치과병원·한방병원 포함)에서 교체·구매 가능한 품목을 우선 지원
* 의료기기법 제2조 제1항(정의)에 해당되는 제품으로, 대학병원 등 종합병원급 시장에 진입하여 국산점유율 상승이 가능하며 식약처신고·인증·허가 완료된 제품
- 주관기관은 다수의 제품을 평가할 경우, 별도의 컨소시엄을 구성하여 신청(단, 연구책임자 1인당 1과제 신청 가능)
□ 지원 내용
○ 정부는 주관기관이 국산 신제품 평가에 필요한 소요비용(과제당 최대 7,500만원/연 이내, 최대 15,000만원/2년 이내) 지원
- 신제품 평가 인력 인건비, 재료비, 시험비, 의학회 학술발표비 등
* 정부 지원금은 최종 선정된 과제 수, 과제 규모 등을 검토하여 조정될 수 있음
□ 지원 조건
○ (주관기관) 국산의료기기 신제품 평가에 필요한 인력 및 공간, 시설 등을 제공
* 선정된 컨소시엄은 사업 착수 초기(3월 중) ‘의료기기산업 종합지원센터’를 통해 신제품 평가 및 시장진입 절차에 대한 컨설팅 1회 실시
○ (참여기업) 신제품 평가에 필요한 비용의 일부를 기업부담금으로 부담
* 신제품 평가에 필요한 참여기업 제품은 주관기관에 현물로 제공하고, 기업부담금(현금)으로 2,500만원 부담
□ 주요 사업내용
○ 국산 신제품 평가(주관기관)
- 주관기관은 사업기간동안 국산 신제품을 사용하고, 제품의 성능을 평가
* 제품 우수성 입증, 성능 개선 등 명확한 목적을 설정하여 사업종료 후 마케팅, 성능개선 등에 활용될 수 있도록 신제품 평가 계획 수립 및 사업수행
○ 국산 신제품 개선(참여기업)
- 주관기관은 평가 제품을 사용한 의견을 참여기업에 피드백
- 참여기업은 주관기관의 제품 사용 의견을 토대로 평가 제품 개선사항을 받아 성능을 지속적으로 개선
- 참여기업은 평가 제품의 전년, 금년, 차년도 매출액을 11월 말까지 보고
○ 평가 완료 제품의 결과 활용(주관기관-참여기업, 정부)
- 주관기관은 제품 평가를 통해 입증된 제품 우수성을 논문 게재, 의학회 발표, 성과교류회(10월 예정) 발표 등 성과물 창출
- 정부는 신제품 평가 결과를 공개, 참여기업은 신제품 평가결과를 마케팅에 활용
3. 신청기간 및 방법
□ 공고 및 신청기간
○ 2019.12.23 ~ 2020.1.31 (6주간)
□ 신청방법
○ 우편 및 방문접수
- (28159) 충청북도 청주시 흥덕구 오송읍 오송생명2로 187 오송보건의료행정타운 한국보건산업진흥원 5층 의료기기산업팀
- 1.31(금) 18:00 限 도착분에 한함
□ 신청서류
○ 사업신청서(별지 서식) 1부 (전자문서는 e-mail, USB 등의 방법으로 별도 제출)
※ 한국보건산업진흥원 홈페이지(www.khidi.or.kr) 사업공고 등에서 다운로드
○ 공통 구비서류 : 주관기관 및 참여기업 법인등기부등본(또는 사업자등록증) 1부
※ 접수된 자료는 반환하지 않음
□ 문의처
○ 한국보건산업진흥원 의료기기산업지원팀 김서윤 연구원(☎ : 043-713-8707, E-Mail : sykim04@khidi.or.kr)








![[국민권익위원회/ 청탁금지법]](/UploadFiles/common/bannerMgr/1585632946963.gif)








![2020년 대한민국발명특허대전[KIPEX] 출품 신청 안내](/UploadFiles/common/bannerMgr/1597712376125.jpg)


