국내뉴스
home > 국내외뉴스> 국내뉴스
- 글자크기
올릭스, """"GalNAc-siRNA 플랫폼"""" HBV∙NASH 경쟁력은?
| 작성자 | 관리자 | ||
|---|---|---|---|
| 작성일 | 2021-10-07 | 조회수 | 3,370 |
| 출처 | 메디소비자뉴스 | ||
| 원문 | http://www.biospectator.com/view/news_view.php?varAtcId=14231 | ||
바이오스펙테이터 서윤석 기자
동물모델서 OLX703A HBV 항원, DNA 감소, OLX702A NASH 간조직 지방축적∙지방증 개선..경쟁사 GalNAc 기술 초기단계 기술이전 경향
최근 RNAi 치료제의 개발은 GalNAc 플랫폼과 함께 이뤄졌다고 해도 과언이 아니다. 앨라일람(Anylam)이 2018년 LNP를 이용한 최초의 RNAi 치료제 ‘온파트로(Onpattro)’를 내놓은 이후 시판된 3개의 RNAi 약물 ‘기브라리(Givlaari, givosiran)’, 옥슬루모(Oxlumo, lumasiran)’, ‘렉비오(Leqvio, inclisiran)’ 등은 모두 GalNAc 기술이 적용됐다.
이동기 올릭스 대표는 “올릭스는 현재 디서나, 애로우헤드 등 글로벌 수준에 근접하게 개발역량이 확보됐다고 자체적으로 판단하고 있다”며 “향후 6개월~1년 사이 간질환 분야에서 기술이전 등의 성과를 통해 결과를 보여줄 수 있을 것“이라고 말했다.
올릭스(OliX Pharmaceuticals)는 지난해 3월 간을 표적하는 리간드인 GalNAc 기술 특허권과 노하우에 대한 권리를 독점적으로 도입하는 계약을 AMC와 체결했다. GalNAc 기술을 확보한 올릭스는 지난해 6월 유럽 소재 글로벌 바이오텍과 GalNAc을 적용한 asiRNA 간질환 치료제 후보물질 4종을 도출하는 연구개발 계약을 체결했다. 이 대표는 “현재 후보물질 도출은 완료해 파트너사에서 검증하고 있는 단계”라며 “긍정적인 결과가 있을 경우 라이선스 아웃도 가능할 것”이라고 말했다.
GalNac은 간세포 표면의 ASGR(Asialoglycoprotein receptor)를 인식해 siRNA가 세포내 유입(endocytosis)을 유도하는 표지다. 올릭스는 현재 GalNAc 기술을 적용해 B형간염(HBV), NASH, 간섬유화, 비만/제2형 당뇨병 등에 대한 파이프라인을 개발 중이다. 이 중 HBV가 비임상 단계로 가장 앞서 나가고 있다. 이외에도 프랑스 떼아에 기술이전한 안구질환 파이프라인 ‘OLX301A’, ‘OLX301D’와 비대흉터, 탈모 등 다양한 질환에 대한 파이프라인을 개발중이다.
또 올릭스는 코로나19 백신 개발에 성공하며 검증받은 새로운 플랫폼인 mRNA 기반 백신 및 치료제 개발을 위해 자회사 엠큐렉스(mCureX)를 설립했다.
이 대표는 “한국의 IT기업 하면 네이버, 카카오가 나오는 것처럼 한국의 신약개발기업 하면 올릭스라고 할 수 있도록 제약바이오를 대표하는 독자적인 전략을 가진 바이오기업이 될 것”이라고 향후 포부를 밝혔다. 바이오스펙테이터는 올릭스의 GalNAC-asiRNA 개발 현황과 자회사 엠큐렉스 등에 대해 알아봤다.
◆ HBV, NASH 대상 GalNAc-siRNA 긍정적 결과..”향후 6개월~1년사이 이벤트 기대”
① HBV 치료제 후보물질 ‘OLX703A’ “HBV항원∙DNA 100배 이상 감소”
올릭스는 GalNAc 기술을 확보한 후 피하투여 방식을 통해 전달효율 시험을 진행했다. 먼저 GalNAc에 형광물질을 붙인 후 마우스에 투여한 결과 간조직에 잘 전달되며 단회 투여 후 50일간 유전자 억제효력이 지속된 결과를 확인했다. 올릭스는 현재 NASH, B형간염(HBV), 간 섬유화, 비만/제2형 당뇨 등을 적응증으로 GalNac 기반 파이프라인을 개발 중이다. 현재 제일 앞선 것은 HBV 치료제 후보물질 ‘OLX703A’다.
먼저 올릭스가 개발 중인 OLX703A의 마우스 모델 연구결과를 살펴보자. 올릭스는 HBV의 모든 전사체를 타깃하고 있는 OLX703A를 HBV 마우스 모델(AAV-HBV mouse)에 한번 투여하고 28일 후, 혈중 HBsAg, HBeAg 등 B형간염 항원과 HBV DNA 수치를 분석했다. 그 결과 HBV 항원과 DNA가 모두 대조군 대비 100배 이상 감소한 결과를 확인했다. 이 대표는 “경쟁사들의 GalNAc 기반 HBV 치료제들과 유사한 수준으로 기대이상의 결과”라고 말했다.
아직 동물모델을 이용한 초기 연구라는 한계를 가지고 있지만, HBV 항원과 DNA 억제효과 측면에서 긍정적인 결과로 보인다. 또 선두그룹인 디서나(Dicerna), 애로우헤드(arrowhead) 등이 초기 개발단계에서 로슈(Roche), 얀센(Janssen) 등과 수억~수십억 달러 규모로 라이선스아웃하고 공동개발 중인 것도 관심깊게 지켜봐야할 부분이다.
현재 RNAi를 이용해 HBV 치료제를 개발 중인 선두그룹은 로슈(Roche)/디서나(Dicerna), 얀센(Janssen)/애로우헤드(Arrowhead), Vir 등으로 모두 GalNAc을 기반으로 약물을 개발중이다.
HBV는 간암의 주원인으로 전세계적으로 약 3억명이 앓고 있는 것으로 추정되며, 매년 약 80만명 이상이 HBV관련 간질환으로 사망한다. 현재 사용되고 있는 뉴클레오시드 유사체(nucleoside analog) 등 항바이러스 요법은 HBV바이러스의 억제는 가능하지만 환자 혈액 내 있는 HBV 항원인HBsAg와 HBV DNA를 거의 제거하지 못하는 한계가 있어 환자들은 평생 약물을 복용해야 한다.
경쟁사들이 진행중인 임상 결과를 살펴보자. 먼저 디서나가 로슈와 공동개발 중인 ‘RG6346’은 HBV 임상 1상(NCT03772249) 중간분석에서 HBsAg을 유의미하게 감소시켰다. 기존 HBV 약물로 치료받은 경험이 있는 만성 HBV 환자 18명을 대상으로 분석한 결과로, 디서나는 1.5mg/kg, 3mg/kg, 6mg/kg 용량의 RG6346을 월 1회씩 4번 투여 후 치료효과를 분석했다.
RG6346으로 치료받은 HBV 환자 58%(7/12명)는 HBsAg 수치가 100IU/mL 이하로 감소했으며 1.5mg/kg 투여군은 치료 후 448일이 지나도 낮아진 HBsAg 수치(1.4log10IU/mL)가 유지됐다. 다른 용량 투여군은 현재 추적관찰 중이다.
또 디서나와 로슈는 RG6346으로 치료받은 환자들에게서 심각한 부작용(SAE)를 확인하지 못했다. 용량제한독성(DLT)는 관찰되지 않았으며 가장 흔한 부작용은 주사부위 반응이었다.
RG6346은 디서나의 GalXC 플랫폼 기술로 개발됐으며 HBV 유전체의 S부위를 타깃해 HBsAg 형성을 억제하는 기전의 약물이다. 로슈가 디서나로부터 지난 2019년 16억7000만달러에 RG6346을 인수했으며, 이듬해 로슈는 자체 개발 중이던 HBV 치료제 후보물질 ‘RG6004’의 개발중단을 밝혔다.
다음으로 얀센(Janssen)과 애로우헤드(Arrowhead)가 개발중인 ‘JNJ-3989’의 임상 2상 결과를 살펴보자. 얀센은 애로우헤드의 HBV 약물을 지난 2018년 2억5000만달러에 사들여 공동개발 중이다.
얀센과 에로우헤드는 39명의 만성 HBV 환자 39명을 대상으로 기존 뉴클레오시드유사체(NA) 치료제와 병용해 임상을 진행했다. JNJ-3989는 0일, 28일, 56일 3회 투여했으며 투여 후 약 392일간 HBsAg 수치를 추적 분석했다. 그 결과 JNJ-3989를 투여받은 HBV 환자 39%(15/39명)은 392일간 HBsAg가 90% 이상(-2.0log10IU/mL) 감소했으며 HBV 환자 28%(11/39명)은 392일간 HBV RNA 수치가 90%이상 줄어든 상태로 유지됐다.
가장 흔하게 나타난 이상반응은 피로, 복통, 주사부위 반응이었으며, 392일간 약물관련 이상반응은 관찰되지 않았다.
Vir는 HBV 치료제 후보물질 ‘VIR-2218’의 임상 2상에서 HBsAg 수치를 감소시킨 결과를 확인했다. 구체적으로 Vir는 32명의 만성 HBV환자에게 20mg, 50mg, 100mg, 200mg 용량의 VIR-2218을 1일, 29일 2회 투여한 결과, 약 48주까지 용량의존적으로 HBsAg 수치가 감소된 것을 확인했다. 임상과정 중 가장 흔하게 나타난 부작용은 두통(25%) 이었으며 부작용으로 인한 임상중단 사례는 없었다.
Vir는 HBV의 기능적치료(functional cure)를 위해 바이러스를 억제함과 동시에 체내 면역시스템을 활성화해 면역반응을 높이는 접근법을 연구 중인데, VIR-2218을 핵심 약물(Backbone Therapy)로 사용할 계획이다. HBV의 기능적 치료는 치료 종료 6개월 후 혈액내 HBsAg가 0.05 IU/mL 이하이며 HBV DNA가 검출되지 않는 상태를 의미한다.
현재 Vir는 VIR-2218을 체내 면역반응을 활성화하는 ‘PEG-IFN-α’와 HBsAg 항체 ‘VIR-3434’를 각각 병용하는 임상 2상을 진행하고 있다. 또 길리어드(Gilead)와 협력해 면역반응을 높이는 TLR 작용제 ‘GS-9688’과 병용하는 임상 2상을 진행중이다.
②NASH 치료제 후보물질 ’OLX702A’ “마우스모델 지방축적 감소”
다음으로 올릭스가 개발 중인 ‘OLX702A’는 GalNAc 기반의 NASH asiRNA 치료제 후보물질에 대해 알아보자. 이 물질은 올릭스의 과학기술자문위(SAB) 멤버인 애런 하킴(Aaron Hakim) 하버드의대 교수의 자문을 기반으로 GWAS(Genome-Wide Association Study) 분석을 통해 발굴한 신규 NASH 관련 유전자를 타깃한다. 상세 타깃에 대해서는 공개하지 않았다.
이 대표는 “과학자문위원인 하킴 교수와 긴밀한 토론을 거쳐 후보물질을 선정해 연구를 진행했다”며 “타깃 유전자를 넉다운(KO) 시키면 NASH로 진행이 안되게 하는 컨셉으로 경쟁사에서 개발중인 타깃과는 다른 것”이라고 말했다. 이어 “하킴 교수는 우리 후보물질에 대한 논문은 아니지만, 간질환에 대한 GWAS기반 연구 결과를 논문으로 게재하기도 했다”고 덧붙였다.
하킴 교수는 영국 바이오뱅크(UK Biobank)와 General Brigham BioBank를 이용 GWAS 분석을 통해 GPAM(mitochondrial glycerol-3-phosphate acyltransferase)을 발굴했다. GPAM은 간손상 지표인 ALT(alanine aminotransferase), AST(aspartate aminotransferase), ALP(alkaline phosphatase) 등의 증가와 관련이 높았다. 하킴 교수는 GPAM이 알코올성 간질환(Alcoholic liver disease), 지방간질환(fatty liver disease) 등과 관련이 있어 만성 간질환에 대한 치료제로의 표적 가능성을 제시했다(doi:10.1002/hep.32038).
올릭스는 마우스 모델에 OLX702A를 투여한 결과 NASH의 주요증상으로 알려진 지방축적(lipid droplet)과 지방증(lipidosis) 개선을 확인했다. 또 고지방식을 먹인 마우스모델에서 대조군 대비 마우스 무게가 10%이상 감소한 결과를 관찰했다. 지방이 덜 축적됐다고 볼 수 있는 결과다.
실제로 마우스 모델의 간조직에 축적된 지방은 oil red O 염색 결과 정상수준으로 개선됐다. 간조직의 지방증도 대조군 대비 확연하게 감소된 조직분석 결과를 보였다. 또 OLX702A를 투여한 마우스는 대조군과 비교해 간손상표지인자, 혈중지질 농도인 콜레스테롤, LDL 등이 감소하는 경향(favorable changes)을 보였다고 올릭스는 설명했다.
NASH는 알코올 섭취 이외의 이유로 간에 지방이 축적되면서 염증이 발생하는 만성염증질환이다. NASH로 인해 간 기능 손상이 진행되면서 간경변이나 간암으로 발전하게 된다. 현재까지 미국 식품의약국(FDA)에서 승인된 NASH 치료제는 없는 상황이다. 최근에는 수년간 유망한 NASH 치료제라 생각되던 약물들이 연달아 임상 실패 소식을 전해오며 NASH 치료제 개발의 어려움을 보여줬다.
인터셉트(Intercept Pharmaceuticals)는 지난해 NASH 치료제로 기대됐던 ‘OCA(obeticholic acid)’를 미국 식품의약국(FDA)에서 이점 대비 리스크가 크다는 이유로 시판 거절당했다. 간 섬유화증은 개선했으나 이상반응으로 인해 약 15%의 환자는 임상을 중단했다.
앨라일람(Anylam)/리제네론(Regeneron), 애로우헤드 등은 RNAi를 이용한 NASH 치료제 후보물질의 임상 1상을 진행중이다. 두 회사 모두 HSD17B13 유전자를 표적으로 치료제를 개발중이다. HSD17B13은 스테로이드 대사와 관련된 효소인 17β-Hydroxysteroid Dehydrogenase 13 단백질을 암호화(coding)하고 있는 유전자다.
기존 연구에 따르면 약 4만6544명의 간 질환 환자의 건강기록과 유전체 서열을 분석한 결과, HSD17B13 유전자 변이를 가진 환자의 경우 간 손상 정도를 나타내는 ALT와 AST 농도가 낮았다. 또 HSD 변이를 가진 환자는 알코올성간질환 위험은 42~53%, 비알코올성간질환(Nonalcoholic Liver Disease) 위험성은 17~30% 감소했다. 알코올성간경변(alcoholic cirrhosis)과 비알코올성 간경변(nonalcoholic cirrhosis) 위험성은 각각 42~73%, 26~49% 줄어들었다. 또 NASH 위험성 감소와도 관련이 있었다는 설명이다(doi: 10.1056/NEJMoa1712191).
앨라일람과 리제네론은 지난 2018년 파트너십을 맺고 HSD17B13 타깃 NASH RNAi 치료제 후보물질 ‘ALN-HSD’를 개발중이다. ALN-HSD는 HSD17B13의 발현을 낮춰 간조직의 염증반응, 상처, 섬유화 등을 감소시켜 치료하는 컨셉이다. 앨라일람은 쥐와 영장류(NHP)에게 ALN-HSD를 투여한 결과 약 6주간 HSD17B13의 mRNA와 단백질 발현이 약 80% 낮아졌다가 점차 회복되는 패턴을 확인했다. 독성과 안전성 이슈도 나타나지 않았다.
앨라일람은 지난해 NASH 환자 128명을 대상으로 임상 1상(NCT04565717)을 시작했으며 올해 말까지 안전성 데이터를 확인할 수 있을 것으로 기대하고 있다.
애로우헤드는 현재 ARO-HSD 임상 1상을 진행 중이다. 애로우헤드는 건강한 임상참여자 32명을 대상으로 ARO-HSD를 25mg, 50mg, 100mg, 200mg, NASH 환자 5명에게는 ARO-HSD 100mg을 투여해 안전성과 효과를 분석했다. NASH환자들은 ARO-HSD 투여 후 71일차 분석에서 HSD17B13 mRNA 수치는 평균 83.8%, 단백질 수치는 83.6% 이상 감소했다. ALT 수치도 기준선(평균) 76에서 약 45.6% 감소했으며, 간 지방증 지표인 MRI-PDFF는 평균 3.9% 줄어들었다. ARO-HSD 투여시 나타난 이상반응은 대부분 경증으로 심각한 이상반응과 약물 관련 이상반응은 관찰되지 않았으며 임상중단자도 없었다.
이 대표는 “NASH는 아직까지 승인받은 치료제가 없는, 글로벌 제약사들이 주목하고 있는 질환으로 초기단계에서도 기술이전 성사 가능성을 가지고 있다”며 “향후 6개월~1년사이에 HBV와 NASH에 대한 이벤트가 있을 것으로 기대하고 있다”고 말했다.
◆ RNAi 치료제 딜.."초기 개발단계 집중"
앤드류 파이어(Andrw Fire) 스탠포드대 교수와 크레이그 멜로 매사추세츠주립대 교수가 RNAi를 발견한 공로로 2006년 노벨생리학상을 받을 때만 해도 RNAi를 이용한 신약개발에 장밋빛 미래가 펼쳐진 것만 같았다. 그러나 이후 앨라일람이 2018년 최초의 RNAi 약물 ''''온파트로(Onpattro)''''를 시판할 때까지 10년이 넘는 시간이 소요됐다.
기술의 개발과 상업화 사이에는 큰 갭이 있는 것이다. 미국 자문회사인 가트너(Gartner)의 기술 하이프사이클(hype cycle)에 따르면 신기술이 나오고 상업화되기까지 일정한 패턴이 나타난다는 것이다. 하이프사이클은 초기에는 대중의 관심이 집중되는 초기 개념입증 단계, 기대감이 최고조에 이르는 버블단계, 실패 및 관심이 사그라드는 단계, 차세대 기술이 개발되며 투자가 집중되는 단계, 혁신 기술이 주류가 되는 단계 등 5단계로 구분된다.
RNAi 약물의 개발 역사도 유사했다. 초기인 2004년에는 RNAi 임상이 처음으로 시도되고 미국 머크(MSD) 등이 당시 선두주자였던 SiRNA Therapeutics 등을 11억달러에 인수하기도 했다. 하지만 임상개발 실패가 이어지며 2010~2013년 사이 로슈 머크 등 글로벌 제약사들이 개발에서 손을 떼기 시작했다. 이후 LNP, GalNAc 등이 개발되면서 투자가 집중되고 RNAi 신약이 나오게 된 것이다.
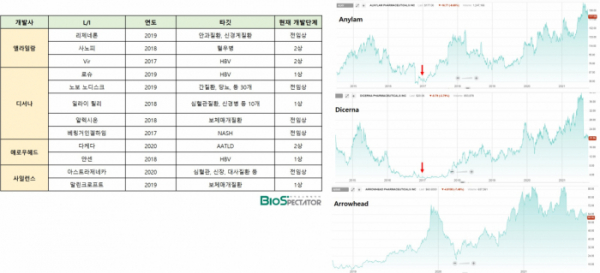
실제로 글로벌 제약사 간 RNAi 약물 개발 딜을 살펴보면 앨라일람의 온파트로에 대한 승인 기대감이 올라간 2017~2020년 사이 집중됐다. 먼저 앨라일람은 2017년 Vir와 B형간염 등의 감염병 치료제 개발을 위해 10억달러 규모 딜을 체결했다. 이어 2018년 사노피와 혈우병 치료제, 2019년 리제네론과 안과질환, 신경계질환 치료제 개발을 위해 10억달러 규모의 계약을 체결했다.
디서나는 2017년 베링거인겔하임과 NASH 치료제 개발을 위해 2억달러, 2018년 일라이 릴리와 심혈관 대사질환, 신경병성질환 등 10개 적응증에 대해 타깃당 3억5000만달러 규모의 딜을 체결했다. 2019년에는 노보노디스크와 간질환, 당뇨 등 30개 적응증에 대해 타깃당 3억6000만달러 규모의 딜을, 로슈와는 B형간염 치료제 개발을 위해 17억달러 규모 기술이전을 진행했다.
애로우헤드는 2018년 얀센과 B형간염 약물을 3억달러에 라이선스아웃했고, 2020년에는 다케다와 AATLD 간질환 치료제 개발을 위해 10억달러 규모 계약을 체결했다.
이런 RNAi 약물들의 기술이전은 전임상과 임상 1상 등 초기단계에서 이뤄진 점이 특징이다. 올릭스의 GalNAc 기반 연구가 초기단계임에도 불구하고 회사측이 기술이전 가능성을 기대하는 이유다. 또 로슈(Roche), 애브비(Abbvie), 화이자(Pfizer), 미국 머크(MSD), BMS, 길리어드(Gilead) 등은 아직 GalNAc 기술에 대한 파트너십을 체결하지 않은 상황이라는 점도 올릭스가 주목하고 있는 포인트중 하나다. 앨라일람, 디서나, 애로우헤드는 주가변화 추이를 살펴보면 RNAi 치료제 시판이 가시화되거나 GalNAc을 기반으로 기술이전 등이 이뤄진 후부터 상승세로 전환된 경향을 볼 수 있다.
◆ mRNA 백신 치료제 개발사 엠큐렉스 설립..”RNAi를 넘어 mRNA까지 total RNA 치료제 개발기업으로 성장할 것”
엠큐렉스는 올릭스가 mRNA 백신∙치료제를 개발하기 위해 설립한 회사다. 홍선우 엠큐렉스 대표는 올릭스 기업부설연구소장을 겸직하고 있으며, 연구 총괄(CTO)은 신동원 박사가 담당하고 있다. 신 박사는 20여년간 mRNA 및 올리고 핵산 연구경력을 가진 mRNA 분야 전문가로 미국 트라이링크 바이오테크놀로지(Trilink Biotechnologies)를 거쳐 올릭스 미국지사에서 mRNA 기술을 포함한 핵산 관련 연구개발을 해왔다.
이 대표는 “mRNA 약물을 개발하는 핵심 요소는 mRNA 구조, 전달체 기술, 생산기술 등으로 구분할 수 있다”며 “엠큐렉스는 mRNA 생산 정제 기술과 분석기술에 관한 노하우를 보유하고 있다”고 말했다.
엠큐렉스의 첫 파이프라인은 코로나19 백신 ‘MCX101’이다. 코로나19 바이러스의 스파이크단백질(S protein)을 항원으로 개발 중이다. 기존에 개발된 화이자/바이오엔텍(Pfizer/BioNtech), 모더나(Moderna)의 코로나19 백신에 사용된 mRNA 특허를 침해하지 않는다는 설명이다. 엠큐렉스는 올해 하반기 코로나19 mRNA 백신 후보물질의 전임상에 진입할 계획이다. 이후 순차적으로 독감 등 감염성 질환, 항암백신과 호흡기질환, 간질환에 대한 mRNA 치료제 후보물질 개발을 진행할 예정이다.
엠큐렉스는 지난 6월 아주IB투자, 키움인베스트먼트 등으로부터 45억원, 올릭스, 피씨엘, 삼양홀딩스 등을 대상으로 25억원의 전략적투자를 유치했다. 엠큐렉스는 이 자금을 바탕으로 코로나19 백신 연구개발을 진행할 예정이다.