국내뉴스
home > 국내외뉴스> 국내뉴스
- 글자크기
엠디뮨, 세포유래 소포체(CDV) """"바이오드론"""" 약물전달
| 작성자 | 관리자 | ||
|---|---|---|---|
| 작성일 | 2021-03-31 | 조회수 | 2,203 |
| 출처 | 메디소비자뉴스 | ||
| 원문 | http://www.biospectator.com/view/news_view.php?varAtcId=12793 | ||
바이오스펙테이터 서윤석 기자
대량생산 가능, 엑소좀보다 균일한 특성(homogenous)으로 다양한 CDV 가능..론자와의 파트너링 선정이 터닝포인트, 해외서 파트너십 문의 잇따라 최근 2건 체결..만성폐쇄성질환(COPD) 및 항암제 탑재 CDV 개발 중
배신규 엠디뮨 대표는 “원하는 사람에게, 원하는 약물을, 원하는 곳에 전달하는 기술을 개발하는 것이 목표”라며 “이를 위해 엑소좀(exosome)과 유사한 세포유래 소포체(cell-derived vesicle, CDV)를 이용한 ‘바이오드론(Biodrone)’ 약물전달 기술을 연구하고 있다”라고 말했다.
지난 2015년 설립된 엠디뮨은 세포유래 소포체(CDV) 이용한 바이오드론 플랫폼 기술과 이를 이용한 파이프라인을 개발하고 있다. 배 대표는 “CDV는 엑소좀과 유사하면서도 독특한 특징을 가지고 있다”며 "대량 생산이 가능하고, 엑소좀보다 균일한 특성(homogenous)을 가지고 있으며, 세포의 종류와 관계없이 CDV를 제조할 수 있다는 것이 장점"이라고 강조했다.
엑소좀은 세포에서 분비되는 80~150nm 크기의 소포체다. 엑소좀은 세포내에서 분비되는 양이 적어 대량으로 생산하는데에는 한계가 있는 반면, 엠디뮨의 압출방식은 소량의 세포에서 다량의 CDV를 얻을 수 있을 뿐 아니라, 다양한 세포를 이용해 생산이 가능한 장점을 가진다는 설명이다.
이런 점에서 엑소좀 기반 신약을 개발 중인 에복스(Evox), 코디악(Codiak Bioscience)과는 결이 다르다. 에복스와 코디악은 엑소좀에 저분자화합물과 DNA, RNA와 같은 핵산치료제를 탑재해 타깃 조직에 전달하는 방식으로 약물을 개발하고 있다. 코디악은 리드 파이프라인의 임상1상을 진행하고 있으며, 에복스는 임상을 준비 중에 있다.
그럼에도 에복스는 다케다(Takeda), 일라이릴리(Eli lilly), 베링거인겔하임(Boehringer Ingelheim) 등과, 코디악은 재즈(Jazz Pharamceuticals), 사렙타(Sarepta Therapeutics) 등과 수천만~수억달러 규모의 연구개발 파트너십을 체결하며 엑소좀 기반 치료제에 대한 기대감을 보여주고 있다.
엠디뮨은 다양한 조직 기반의 줄기세포를 이용해 CDV를 제조하는 기술을 확보하고 있다. 줄기세포 유래 CDV는 줄기세포가 가진 세포재생효과를 가지고 있어, 엠디뮨은 이를 이용해 다양한 질환에 적용하는 연구를 진행하고 있다. 또, 엠디뮨은 CDV에 저분자화합물, 화학항암제, 핵산 등을 탑재해 치료효과를 높인 항암제를 개발하고 있다.
배 대표는 "우리는 PIDO(platform inside development outside) 사업모델을 추구한다"며 "PIDO는 플랫폼 기술을 기반으로 내부에서 원천기술을 개발하고, 임상은 외부에서 진행해 기술이전을 통해 수익을 내는 모델"이라고 말했다.
현재, 엠디뮨은 Pre-IPO 투자유치를 준비하고 있으며, 올해 말까지 코스닥시장 상장을 위한 준비작업을 마칠 계획이다. 바이오스펙테이터는 엠디뮨의 바이오드론 약물전달 기술과 개발 중인 파이프라인에 대해 알아봤다.
◆ 포인트 1. 세포유래 소포체(CDV) 이용 약물전달 기술..”바이오드론”
엠디뮨의 핵심기술은 다양한 세포에서 압출법을 통해 세포유래 소포체(CDV)를 이용한 약물전달 플랫폼 ‘바이오드론’이다. 배 대표는 “특정 조직의 세포에서 압출한 CDV는 같은 부위로 이동하는 트로피즘(tropism)이 있다”며 “이를 이용해 원하는 곳에, 원하는 약물을 전달할 수 있는 것”이라고 말했다.
엠디뮨은 압출방식의 장점으로 △대량생산이 가능하고 △다양한 세포를 사용할 수 있다는 점을 꼽았다. 배 대표는 "기존에 엑소좀을 얻기 위해 사용하던 줄기세포배양법에 비해 10~100배 이상 많은 양을 생산할 수 있다"며 "이는 세포를 조그만한 구멍을 통해 압출하면서 하나의 세포가 여러 개의 소포체로 쪼개지기 때문"이라고 압출방식에 대해 설명했다.
이렇게 쪼개진 소포체에는 다양한 바이오마커를 비롯해 여러 단백질들을 가지고 있으며, 약물도 탑재할 수 있다. 또, 세포를 압출하는 방식이기 때문에 모든 조직의 세포를 동일한 조건에 적용할 수 있다. 기존에는 세포의 종류에 따라 배양조건들이 달라지는 어려움이 있다. 특히, 특정 조직의 세포들로부터 압출한 소포체는 같은 부위로 이동하는 특성이 있다. 여기에 특정 리간드 또는 바이어마커 등을 엔지니어링하게 되면 표적화 능력을 높여 원하는 곳에, 원하는 약물을 전달할 수 있다는 설명이다. 이 때문에 엠디뮨은 이를 ‘바이오드론’이라고 명명한 것.
엠디뮨은 2015년 포항공대에서 개발된 ‘세포유래 베지클 원천특허’를 이전해왔다. 포항공대 연구팀은 압출방식을 이용해 혈구암세포주인 U937과 대식세포인 Raw264.7에 화학항암제인 독소루비신(doxorubicin)을 탑재하고 10㎛, 5㎛, 1㎛ 필터로 압출해 약물이 탑재된 엑소좀 유사 나노소포체(exosome-mimetic nanovesicles, NV)를 추출했다(doi: 10.1021/nn402232g).
이후 종양모델에 Raw264.7세포에서 추출한 소포체와 독소루비신을 탑재한 소포체를 투여한 결과, 독소루비신이 탑재된 소포체를 투여한 경우 종양크기가 최대 4분의 1수준으로 작아졌다. 또, 마우스모델의 암세포에서 세포분열과 세포사멸이 유도된 결과를 확인했다(doi: 10.1021/nn402232g). 독소루비신은 대표적인 화학항암제로 DNA 복제와 RNA 전사를 억제하기 때문이다.
특히, CDV에 독소루비신을 탑재할 경우 적은 용량에서도 효과적이고 독성이 적은 항암효과를 보였다. 구체적으로, 종양모델에 독소루비신을 15㎍, 60㎍ 용량으로 단독 또는 Raw264.7 유래 CDV(Raw264.7-CDV)에 독소루비신 3㎍을 탑재해 투여했다. 그 결과, 60㎍용량의 독소루비신을 투여군과 Raw264.7-CDV+3㎍ 독소루비신 투여군에서 종양크기가 유사한 수준으로 감소한 결과를 확인했다(doi: 10.1021/nn402232g). 또 Raw264.7-CDV+3㎍ 독소루비신을 투여했을 때 독소루비신 60㎍에서 나타나는 백혈구 감소, 체중감량 등의 독성이 나타나지 않았다.
배 대표는 “암세포에 대한 타깃능력을 높여 낮은 용량으로도 고용량의 단일약물과 동일한 효능을 보일뿐 아니라 독성 문제도 줄일 수 있다는 의미”라고 말했다. 이런 결과를 기반으로 엠디뮨은 현재 면역세포인 NK세포 기반 CDV에 다양한 항암제를 탑재해 효과를 평가하는 연구를 진행하고 있다.
◆ 포인트 2. 론자(Lonza)와의 파트너링..”터닝포인트가 될 것”
배 대표는 “지난해 스타트업 인큐베이팅 프로그램에서 론자(Lonza)의 파트너로 선정된 것이 큰 기회가 됐다”고 말했다. 엠디뮨은 지난해 10월 플러그앤플레이(Plug and Play)가 주최한 글로벌스타트업 인큐베이팅 프로그램인 ‘Startup Creasphere Program’에서 글로벌 CMO 업체인 론자의 파트너로 선정됐다. 엠디뮨이 참여한 배치5(Batch 5)에는 사노피(Sanofi), 론자, 로슈(Roche) 등이 직접 선정한 11개 기업이 공동 프로젝트를 12주간 진행하게 되는데 여기에 선정된 것.
론자는 엠디뮨 선정이유로 바이오드론 기술을 꼽았는데, 다양한 세포로부터 압출을 통해 기존 엑소좀 대비 10~30배 많은 양의 CDV 대량생산 기술을 가진 것이 주효했다는 설명이다.
배 대표는 “론자는 엑소좀 생산기술에 관심이 높은 편인데, 우리의 기술에 주목해 파트너로 선정됐다"며 "12주간의 프로젝트가 완료된 이후 현재 추가 협력논의를 진행하고 있는 상황”이라고 말했다. 이어 “론자와 파트너링 이후, 이전보다 글로벌 바이오텍에서 파트너십 문의가 더 들어오고 있다”고 말했다.
이 때문일까? 엠디뮨은 이달에만 2건의 파트너십을 체결했다. 먼저, 엠디뮨은 미국 엑소나노RNA(ExonanoRNA)와 약물전달 표적화 기술을, 오스트리아 에버사이트(Evercyte GmbH)와 항암제 전달 표적화 연구개발을 위한 파트너십을 체결했다.
엑소나노RNA는 RNA 나노입자를 부착해 조직 및 세포에 약물을 전달하는 기술을 보유하고 있고, 에버사이트는 테트라스파닌(tetraspanin) 막단백질 변이를 통한 타깃팅 기술을 가지고 있다. 엠디뮨은 바이오드론 플랫폼과 이들 회사의 기술을 합쳐 원하는 조직/암세포에 약물을 전달하는 시스템을 개발할 계획이다.
◆ CDV 기반 COPD 치료제 후보물질..마우스 모델서 “폐 세포 재생효과”
배 대표는 “항암제를 제외하면 우리 파이프라인은 전부 줄기세포 자체의 재생효과를 이용해 개발하고 있다”며 “리드 파이프라인은 희귀 난치질환인 만성폐쇄성폐질환(COPD)을 타깃하는 CDV 기반 약물”이라고 개발중인 파이프라인을 소개했다.
WHO에 따르면 만성폐쇄성폐질환은 2020년 기준 사망원인 3위인 질병이다. 만성적인 염증반응으로 인해 기도가 좁아지는 진행성 질환이다. 폐활량의 감소로 체내 산소공급이 감소하고, 만성적인 기침 및 객담이 동반되며, 기관지 경련으로 호흡곤란이 나타나게 된다. 만성폐쇄성폐질환은 비가역적으로 기도가 좁아져 기도확장이 불가능하기 때문에 증상의 악화를 지연시키는 것이 목표다. 현재까지 손상된 폐 세포를 재생하는 컨셉의 치료제는 없는 상황이다.
엠디뮨은 아산병원 연구팀과 COPD 치료제 후보물질의 전임상 연구를 진행하고 있다. 아산병원 연구팀은 엘라스타아제(elastase)로 폐손상을 유도한 폐기종(emphysema) 마우스 모델에 지방줄기세포(adipose-derived stem cells, ASCs), ASCs-CDV, 1/3 농도의 ASCs-CDV를 투여했다.
그 결과, ASCs, ASCs-CDV, 1/3 ASCs-CDV를 투여했을 때 모두 엘라스타아제와 비교해 폐세포 유의미한 폐세포 재생효과를 보였고, 특히 1/3 ASCs-CDV를 투여했을 때 폐세포 재생효과가 가장 좋았다. 추가로, ASCs와 ASCs-CDV가 성장인자 신호전달(growth factor signaling)을 자극하는지 알아본 결과, 1/3 ASCs-CDV에서 FGF2 단백질양이 정상수준으로 엘라스타아제 투여군과 비교해 유의미하게 증가한 것을 확인했다. ASCs를 투여했을때는 유의미하진 않지만 FGF2 단백질량이 증가하는 경향을 나타냈다(doi:10.1038/emm.2016.127).
연구팀은 ASCs-CDV가 수용체 의존 세포내이입(receptor-mediated endocytosis)기전을 가진다는 것을 밝혔다. 세포흡수(macroponcytosis), 세포내이입(endocytosis), 식세포작용(phagocytosis), 수용체 의존 세포내이입에 대한 저해제를 투여해 실험한 결과다.
엠디뮨은 그외에도 국내 대학병원 연구팀과 염증성장질환(IBD)을 타깃해 파이프라인을 개발하고 있다. 엠디뮨은 DDS(dextran sodium sulfate)로 유도한 IBD 마우스모델에 ADMSs-CDV를 투여한 결과, 염증 증상이 완화되고, 생존률이 개선된 결과를 확인했다. 특히, ADMSs를 투여한 경우에는 유의미한 개선효과를 보이지 못하는데 반해, ADMS-CDV는 유의미한 치료효과를 보였다는 점이 주목할만하다.
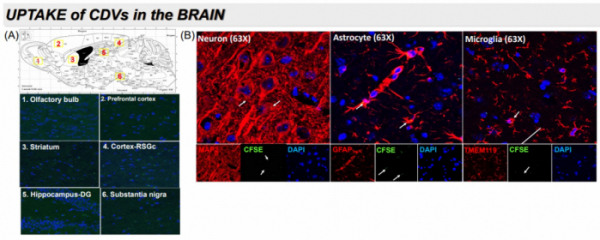
엠디뮨이 지난해 국제 엑소좀학회(ISEV)에서 발표한 포스터를 살펴보면, 마우스에 녹색형광을 붙인 CFSE(carboxyfluorescein succinimidyl ester)로 표지된 ASC-CDV를 비강내 투여해 뇌로 침투하는지 연구했다. 그 결과, 전전두엽피질(prefrontal cortex), 해마(hippocampus), 흑질(substantia nigra), 후구(olfactory bulb) 등 6곳에 ASC-CDV가 혈뇌장벽(BBB)를 통과해 전달된 것을 확인했다.