전체
home 알림마당 기관별 공지사항 전체
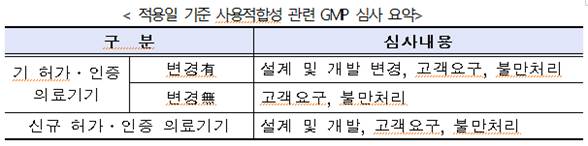
사용적합성 관련 GMP 심사 방안 안내
| 작성자 | 관리자 | ||
|---|---|---|---|
| 작성일 | 2020-12-09 | 조회수 | 6,116 |
| 출처 | 한국의료기기산업협회 | ||
| 원문링크 | http://www.kmdia.or.kr/board/board_10V.asp?mode=VIEW&bid=notice&bidsrl=2&bidssrl=5&intseq=11023 | ||
| 첨부파일 | |||
안녕하세요, 한국의료기기산업협회입니다.
식약처(의료기기관리과)에서는 GMP 기준 중 오는 '21.1.1부터 등급별로 적용되는 사용적합성 요구사항과 관련하여,
사용적합성 관련 GMP 심사 방안을 첨부와 같이 마련하여 시행하고자 합니다.
이에 첨부 및 다음과 같이 안내드리오니, 업무에 참고하여 주시기 바랍니다.
|
사용적합성 관련 GMP 심사 방안 ○ 주요내용 - 적용대상 : '21.1.1 이후 신청한 GMP 심사 - 적용일자 : '21.1.1(4등급) → '21.7.1(3등급) → '22.1.1(2등급) → '22.7.1(1등급) - 적용기준 : IEC 62366-1 또는 이와 동등 이상의 기준 - 일반원칙 : 사용적합성 적용 적정성(절차 및 활동 결과) 심사 - 기타 : 적용일 미경과 시, 사용적합성 절차 수립토록 행정지도 |
감사합니다.